Kovalentne obveznice prema jonskim obvezama
Sadržaj
- Sadržaj: Razlika između kovalentnih i jonskih veza
- Usporedni grafikon
- Što su kovalentne obveznice?
- Što su jonske veze?
- Ključne razlike
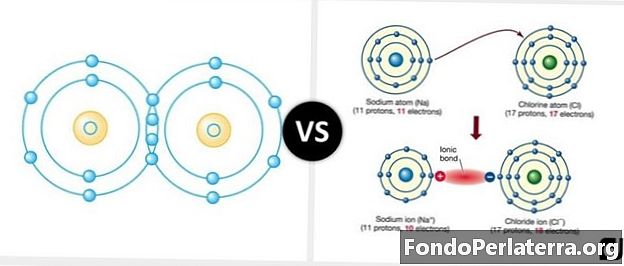
Glavna razlika između ionskih veza i kovalentnih veza je dijeljenje parova elektrona i atoma. U kovalentnim vezama atomi su elektrostatski privlačeni jedni prema drugima dok su u ionskim vezama; parovi elektrona dijele se između atoma.

Sadržaj: Razlika između kovalentnih i jonskih veza
- Usporedni grafikon
- Što su kovalentne obveznice?
- Što su jonske veze?
- Ključne razlike
- Video objašnjenje
Usporedni grafikon
| Osnove razlikovanja | Kovalentne veze | Jonske veze |
| definicija | Kovalentna veza je vrsta kemijske veze koja uključuje dijeljenje zajedničkih parova ili parova (elektronskih parova) između atoma. | Jonska veza je vrsta kemijske veze koja uključuje dijeljenje ili potpuno odustajanje jednog ili više elektrona od jednog atoma do drugog atoma. |
| događaj | Kovalentne veze rezultat su interakcije neutralnih atoma | Ionske veze rezultat su interakcije aniona i kationa. |
| Kemijski potencijal | To su prilično slabe kemijske veze | To su najjača vrsta kemijske veze. |
| formacija | Nemetalni elementi tvore kovalentne veze | Metalni elementi tvore ionske veze |
| Status elektrona | Dijeljeni elektroni | Ukupni prijenos elektrona |
| Stanje materije | Tekućine i plinovi na sobnoj temperaturi | Čvrsta tvar na sobnoj temperaturi |
| spojevi | Organski | Anorganski |
| Topljivost | Netopljivo u vodi | Topiv u vodi |
| Oblik | Definitivan oblik | Nema određenog oblika |
| imenovanje | Grčki prefiksi | Rimski brojevi |
| Primjeri | Hidrokloridna kiselina i metan | Sumporna kiselina i Natrijev klorid |
Što su kovalentne obveznice?
Kovalentne veze, poznate i po nazivu molekularnih veza, vrsta su kemijskih veza koje uključuju dijeljenje zajedničkih parova ili parova povezivanja (parova elektrona) između atoma. U većini molekula dijeljenje elektrona omogućuje svakom atomu da dobije ekvivalent pune vanjske ljuske, što odgovara stabilnoj elektroničkoj konfiguraciji. Ako atomi imaju sličan afinitet za elektrone, vjerojatno će se pojaviti kovalentne veze zbog istog afiniteta prema elektronima i nema tendencije da ih doniraju atomi. Atomi dijele elektrone kako bi dobili konfiguraciju okteta i postali stabilniji i jači. Zbog interakcija sigme i pi orbitale, kovalentne veze mogu tvoriti četiri vrste veza, i to jednostruke, dvostruke, trostruke i četverostruke. Atomi kisika su najbolji primjer koji za stvaranje zatvorene ljuske zahtijeva dva dodatna elektrona, dok vodikovim atomima treba jedan da bi stvorio zatvorenu ljusku. Atom kisika dijeli dva njegova elektrona s atomima vodika, tako da su atomi oba zatvorena ljuska. To u konačnici stvara molekulu vode.
Što su jonske veze?
Jonska veza je vrsta kemijske veze koja uključuje dijeljenje ili potpuno odustajanje jednog ili više elektrona od jednog atoma do drugog atoma. Ionske veze rezultat su onih elemenata koji lako gube elektrone i onih elemenata koji dobivaju elektrone. Ove vrste veza uopće ne predstavljaju molekule zbog interakcije između naboja kako je opisano u Coulombovom zakonu. Jonske veze ostaju čvrste na sobnoj temperaturi jer je, tijekom periodičnih rešetki s milijardama iona, svaki ion okružen mnogim ionima suprotnog naboja. Elektrostatička privlačnost između negativnih i pozitivnih iona spoj drži zajedno. Ukupna energija tijekom procesa ionskog vezivanja normalno je pozitivna što ukazuje na to da je reakcija endotermična i nepovoljna. S druge strane, ova je reakcija istodobno povoljna zbog elektrostatičke privlačnosti. Čest primjer ionske veze je natrij ili sol. Atomi natrija brzo daju elektrone koji rezultiraju pozitivnim nabojem. Klor prihvaća ove elektrone i negativno nabijen. Ta dva nasuprotno nabijena atoma zatim privlače jedan drugog kako bi formirali molekulu natrijevog klorida.
Ključne razlike
- U kovalentnim vezama elektronske se orbitale preklapaju, dok su u slučaju ionskih veza odvojene.
- Kovalentne veze su relativno meke u usporedbi s ionskim vezama koje su tvrde i krhke.
- I atomi metala i nemetalni atomi sudjeluju u stvaranju ionskih veza, dok u stvaranju kovalentnih veza; uključeni su samo atomi ne metala.
- Kovalentne veze nastaju zbog dijeljenja elektrona dok stvaranje ionskih veza nastaje zbog prijenosa elektrona.
- Molekule su čestice u kovalentnim vezama tijekom stvaranja spoja, dok su ionske veze ioni pozitivno nabijeni i negativno nabijeni.
- Kovalentne veze su neprovodnici, dok su ionske veze provodnici.
- Kovalentno vezivanje događa se između atoma malo različitih u elektronegativnosti. Ionsko vezivanje događa se između atoma velike razlike u elektronegativnosti.
- Ionske veze zahtijevaju visoko talište i vrelište u slučaju ionskog vezivanja. Kovalentne veze zahtijevaju nisku talište i vrelište u slučaju kovalentnog vezivanja.
- Metan i klorovodična kiselina uobičajeni su primjeri kovalentne natrijeve kloride i sumporne kiseline primjeri su ionskih veza.
- Kovalentne veze imaju definitivan oblik, dok ionske veze nemaju određeno
- Kovalentne veze imaju malu polarnost, dok ionske veze imaju visok polaritet.
- 100% kovalentne molekule otopit će se u ulju, ali ne i u vodi, dok mnoge ionske veze imaju sposobnost otapanja u vodi, ali ne i u ulju.
- Kovalentne veze važne su jer molekule ugljika djeluju prvenstveno kovalentnim vezama, dok su ionske veze važne jer omogućuju sintezu specifičnih organskih spojeva.
- Kovalentne veze mogu biti i elementi i spojevi, dok ionske veze mogu biti samo spojevi.





