Apsorpcija vs adsorpcija

Sadržaj
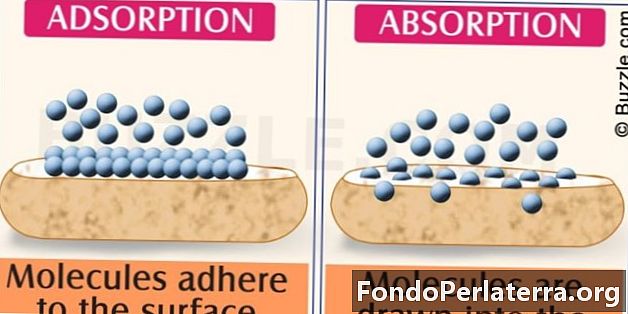
Glavna razlika između apsorpcije i adsorpcije je u tome što je apsorpcija proces u kojem se tekućina otapa ili kruta ili tekuća. Suprotno tome, adsorpcija je proces u kojem se ioni, molekule ili atomi iz tvari poput plina, krute ili tekuće tvari, lijepe na površinu adsorbensa.
Sadržaj: Razlika između apsorpcije i adsorpcije
- Što je apsorpcija?
- Što je adsorpcija?
- Ključne razlike
- Video objašnjenje
Što je apsorpcija?
Apsorpcija je proces u kojem jedna tvar potpuno ulazi u drugu tvar. To je proces u kojem se jedan atom ili molekula usisava unutar volumena drugih molekula. Mora biti dio tvari potpunim ulaskom u nju. To bi mogao biti kemijski ili fizički proces. Na primjer, ugljični dioksid može se apsorbirati u otopinu kalijevog karbonata. Ovo je primjer apsorpcije kemikalije, jer se odvija reakcija. Drugi primjer bi moglo biti otapanje zraka unutar vode. To je fizička apsorpcija budući da zrak ulazi u vodu iz ravnotežnog tlaka. Kada bilo koja tvar ili materijal upije neku količinu tekućine ili plina iznutra, tada se kaže da je taj materijal apsorbirao drugi materijal. Dakle, apsorpcija se u materijalu nešto kreće.
Što je adsorpcija?
Adsorpcija je proces u kojem se plin ili tekućina ne apsorbiraju, već nastaju samo preko površine. Iz sintetskih razloga i pročišćavanja vode, fenomen adsorpcije se široko koristi u industriji. To uključuje adheziju. Tvar se jednostavno zadržava na drugoj tvari u ovom procesu, a da ne ulazi u nju. Na primjer, ugljični dioksid sjedi na površini adsorbensa unutar jedinice adsorbensa za ljuljanje tlaka. Sjedi na površini čvrstog adsorbensa.
Ključne razlike
- Asimilacija molekularnih vrsta u većem dijelu čvrste ili tekućine naziva se apsorpcijom. Akumulacija molekularnih vrsta na površini i ne ulazak u nju naziva se adsorpcijom.
- Apsorpcija je masna pojava dok je adsorpcija površinski fenomen.
- Apsorpcija je endotermički proces, dok je adsorpcija egzotermni proces.
- Temperatura ne utječe na temperaturu, a na adsorpciju pogoduje niska temperatura.
- Apsorpcija se javlja jednoličnom brzinom dok se stopa adsorpcije neprestano povećava i tada konačno postiže ravnotežu.
- Koncentracija je apsorpcija ista u cijelom materijalu. Koncentracija na površini razlikuje se u adsorpciji od one u rasutom stanju.
- Apsorpcija se komercijalno koristi u hladnjacima i pročišćavanju vode.
- Apsorpcija je povezana s volumenom dok je adsorpcija povezana s površinom.
- Apsorpcija uključuje otapanje i difuziju, dok adsorpcija uključuje prijanjanje.
- Pri apsorpciji energiju fotona apsorbira druga cjelina.